初三化学方程式怎么配平一、最小公倍数法适用条件:所配原子在方程式左右各只出现一次。例1:配平:Al+Fe3O4 → Al2O3 +Fe解析:先根据两边氧原子数的最小公倍数是12...
初三化学方程式怎么配平
一、最小公倍数法
适用条件:所配原子在方程式左右各只出现一次。
例1:配平:Al+Fe3O4 → Al2O3 +Fe
解析:先根据两边氧原子数的最小公倍数是12,可确定Fe3O4的系数为3,Al2O3的系数为4。进一步确定Al的系数为8,Fe的系数为9。
结果得:8Al+3Fe3O4 = 4Al2O3 +9Fe
二、奇数配偶法
适用条件:方程式中所配元素的原子个数的奇数只出现一次。
例2. 配平: H2O2→H2O+O2?
解析:方程式中只有水中的氧原子数为奇数,先把H2O的系数配成2。再根据氢原子数确定H2O2的系数为2,最后确定O2的系数为1。
配平结果:2H2O2=2H2O+O2

九年级上册化学配平三种方法
化学方程式的必须遵守质量守恒定律,即反应前后各元素的原子个数相等,这是化学方程式配平的依据.化学方程式的配平方法有很多:如最小公倍数法、奇数配偶法、氧化还原法、 得失电子法,这些方法老师上课都能讲过,如果这些方法都不能满足你的需要,还有一种方法可以解决全部类型的配平,特别是有机物燃烧的配平,即列方程(组)的方法.
aFeS2+bO2=cFe2O3+dSO2
每种元素原子前后个数相等,即列方程:a=2c,2a=d,2b=3c+2d,
解得b=11/4*a,c=1/2*a,d=2a,
所以a=4,b=11,c=2,d=8
abcd之比是最简整数比.
4FeS2+11O2=2Fe2O3+8SO2

初三化学方程式配平的技巧有哪些
1:1. 化学方程式配平的技巧主要包括理解化学方程式的平衡原理和化学反应的物质守恒定律。
这是明确的。
2. 配平化学方程式的原因是为了满足质量守恒和电荷守恒的要求,确保反应前后物质的种类和数量保持不变。
。
3. 在具体的配平过程中,可以采取以下一些技巧: a. 首先,观察方程式中的元素,找出发生变化的元素以及其在反应物和生成物中的数量差异,并以此为基础进行配平。
b. 其次,根据元素的种类和数量差异,调整反应物和生成物的系数,使其正好相等,同时注意不改变反应物的相对比例。
c. 进一步调整系数,确保化学方程式中所涉及的各种原子数目平衡,同时保持反应物和生成物的相对比例不变。
d. 最后,检查配平后的方程式是否满足质量守恒和电荷守恒的要求,若符合要求则配平完成,否则继续调整系数直至平衡。
。
根据1,以上是对初三化学方程式配平技巧的问题的回答。
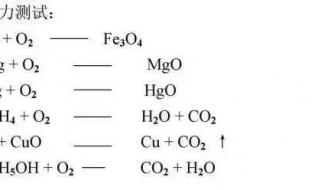
初中化学方程式配平方法和技巧
最小公倍数法
本法也是配平化学反应方程式惯用的方法,通常用于较简单的化学方程式的配平,或者作为配平复杂反应的辅助方主。运用此法一般可按下述步骤去进行:
具体步骤
1.首先,找出反应式左右两端原子数最多的某一只出现一次的元素,求出它们的最小公倍数。
2,其次,将此最小公倍数分别除以左右两边原来的原子数,所得之商值,就分别是它们所在化学式的系数。
3.然后,依据已确定的物质化学式的系数、推导并求出它化学式的系数,直至将方程式配平为止。
4.最后,验证反应式。配平是否正确。
初三上册化学方程配平的万能公式法怎么配
初中最小公倍数法就够用了,就是课本中讲的方法。 先寻找反应前后都只出现一次的需要配平的元素,用最小公倍数法使两边都达到最小公倍数。
如: C + Fe2O3 = Fe + CO2 我们找到的是氧元素需要配平。(也可以是铁,但相对较麻烦)
于是就再氧化铁前面配2使左边氧原子个数达到6个;同时在右边二氧化碳前面配3使右边氧原子个数也达到6. C + 2Fe2O3 = Fe + 3CO2 然后再把没有配平铁元素原子配平 C + 2Fe2O3 = 4Fe + 3CO2 然后再把没有配平碳元素原子配平 3C + 2Fe2O3 = 4Fe + 3CO2 (最后再写条件标上气体符号,这里只将配平就不标了。)
初中考来考去都只有那几个方程式,反复多拿来练练就熟了。
本文来自投稿,不代表星智号立场,如若转载,请注明出处:https://yule.xzhi8.com/hot/202402-32860.html



评论列表(1条)
我是星智号的签约作者“巧绿酱吖”希望本篇文章《初三化学方程式配平 初三化学方程式怎么配平》能对你有所帮助!